衡水金卷先享题·摸底卷 2023-2024学年度高三一轮复习摸底测试卷 化学(江西专版)(二)2答案

衡水金卷先享题·摸底卷 2023-2024学年度高三一轮复习摸底测试卷 化学(江西专版)(二)2答案,目前趣答答案已经汇总了衡水金卷先享题·摸底卷 2023-2024学年度高三一轮复习摸底测试卷 化学(江西专版)(二)2答案的各科答案和试卷,获取更多{{papers_name}}答案解析,请在关注本站。
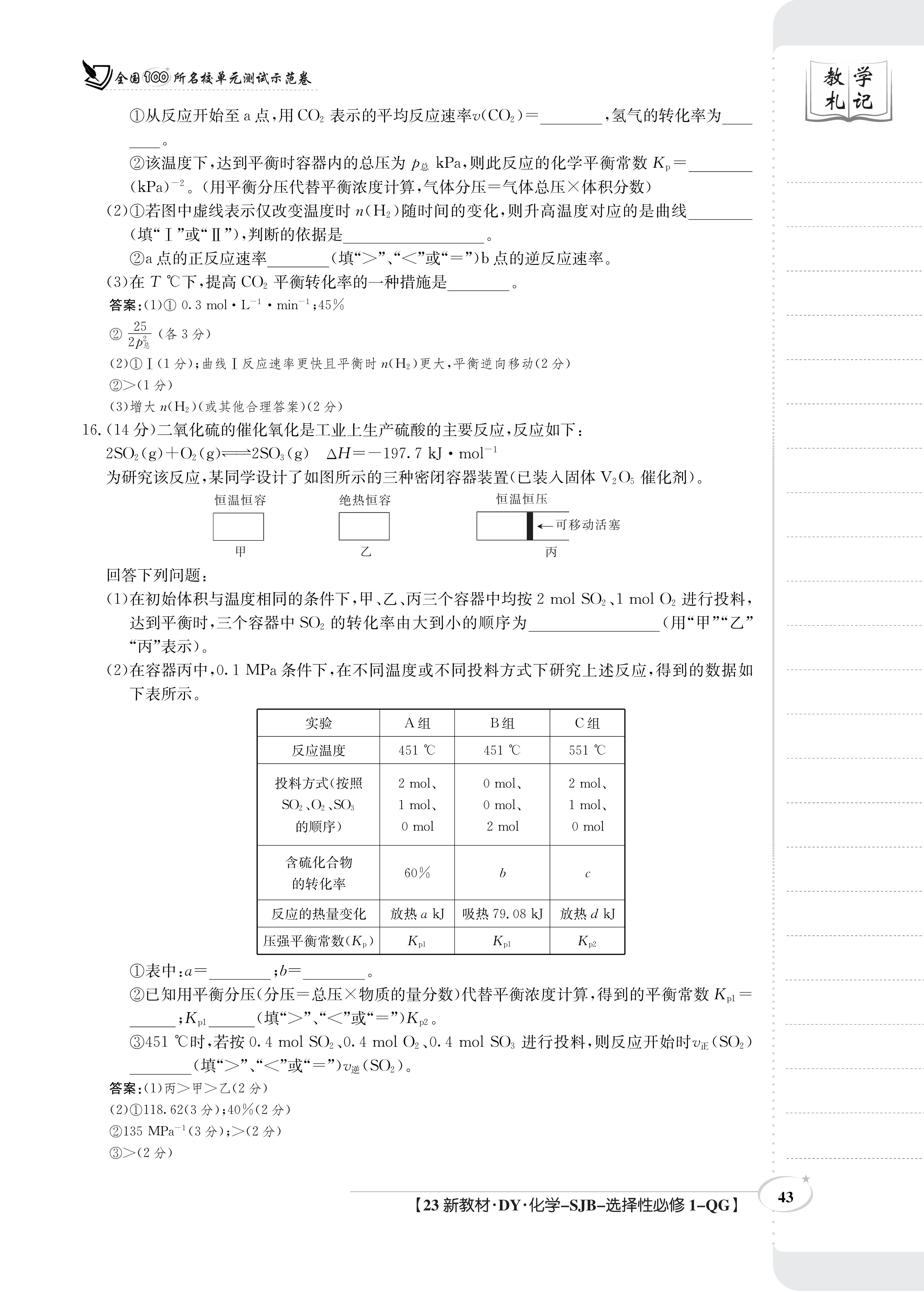 全国@0所名校单元测试示范卷教学①从反应开始至a点,用CO2表示的平均反应速率w(CO2)=,氢气的转化率为札记②该温度下,达到平衡时容器内的总压为p总kPa,则此反应的化学平衡常数K。=(kP)2。(用平衡分压代替平衡浓度计算,气体分压=气体总压×体积分数)(2)①若图中虚线表示仅改变温度时(H2)随时间的变化,则升高温度对应的是曲线(填“I”或“Ⅱ”),判断的依据是②a点的正反应速率(填“>”、“<”或“=”)b点的逆反应速率。(3)在T℃下,提高CO2平衡转化率的一种措施是答案:(1)①0.3mol·L-1·min-1;15%巴器(含3分)(2)①I(1分):曲线I反应速率更快且平衡时(H)更大,平衡逆向移动(2分)②>(1分)(3)增大n(H)(或其他合理答案)(2分)16.(14分)二氧化硫的催化氧化是工业上生产硫酸的主要反应,反应如下:2SO2(g)+O2(g)=2SO3(g)△H=-197.7kJ·mol-1为研究该反应,某同学设计了如图所示的三种密闭容器装置(已装入固体VO催化剂)。恒温恒容绝热恒容恒温恒压←一可移动活塞甲乙丙回答下列问题:(1)在初始体积与温度相同的条件下,甲、乙、丙三个容器中均按2 mol SO2、1molO2进行投料,达到平衡时,三个容器中SO2的转化率由大到小的顺序为(用“甲”“乙”“丙”表示)。(2)在容器丙中,0.1MPa条件下,在不同温度或不同投料方式下研究上述反应,得到的数据如下表所示。实验A组B组C组反应温度451℃451℃551℃投料方式(按照2mol、0mol、2mol、S02、O2、S031mol、0mol、1mol、的顺序)0 mol2 mol0 mol含硫化合物60%b的转化率反应的热量变化放热ak吸热79.08kJ放热dk乐强平衡常数(K,)KplKpKpe①表中:a;b=②已知用平衡分压(分压-总压×物质的量分数)代替平衡浓度计算,得到的平衡常数K;Kpl(填“>”、“<”或“=”)K2。③451℃时,若按0.4 mol SO2、0.4molO2、0.4 mol SO3进行投料,则反应开始时vr(SO2)(填“>”、“<”或“=”)v(SO2)。答案:(1)丙>甲>乙(2分)(2)①118.62(3分);40%(2分)②135MPa1(3分);>(2分)③>(2分)【23新教材·DY·化学-SJB-选择性必修1-QG】43
全国@0所名校单元测试示范卷教学①从反应开始至a点,用CO2表示的平均反应速率w(CO2)=,氢气的转化率为札记②该温度下,达到平衡时容器内的总压为p总kPa,则此反应的化学平衡常数K。=(kP)2。(用平衡分压代替平衡浓度计算,气体分压=气体总压×体积分数)(2)①若图中虚线表示仅改变温度时(H2)随时间的变化,则升高温度对应的是曲线(填“I”或“Ⅱ”),判断的依据是②a点的正反应速率(填“>”、“<”或“=”)b点的逆反应速率。(3)在T℃下,提高CO2平衡转化率的一种措施是答案:(1)①0.3mol·L-1·min-1;15%巴器(含3分)(2)①I(1分):曲线I反应速率更快且平衡时(H)更大,平衡逆向移动(2分)②>(1分)(3)增大n(H)(或其他合理答案)(2分)16.(14分)二氧化硫的催化氧化是工业上生产硫酸的主要反应,反应如下:2SO2(g)+O2(g)=2SO3(g)△H=-197.7kJ·mol-1为研究该反应,某同学设计了如图所示的三种密闭容器装置(已装入固体VO催化剂)。恒温恒容绝热恒容恒温恒压←一可移动活塞甲乙丙回答下列问题:(1)在初始体积与温度相同的条件下,甲、乙、丙三个容器中均按2 mol SO2、1molO2进行投料,达到平衡时,三个容器中SO2的转化率由大到小的顺序为(用“甲”“乙”“丙”表示)。(2)在容器丙中,0.1MPa条件下,在不同温度或不同投料方式下研究上述反应,得到的数据如下表所示。实验A组B组C组反应温度451℃451℃551℃投料方式(按照2mol、0mol、2mol、S02、O2、S031mol、0mol、1mol、的顺序)0 mol2 mol0 mol含硫化合物60%b的转化率反应的热量变化放热ak吸热79.08kJ放热dk乐强平衡常数(K,)KplKpKpe①表中:a;b=②已知用平衡分压(分压-总压×物质的量分数)代替平衡浓度计算,得到的平衡常数K;Kpl(填“>”、“<”或“=”)K2。③451℃时,若按0.4 mol SO2、0.4molO2、0.4 mol SO3进行投料,则反应开始时vr(SO2)(填“>”、“<”或“=”)v(SO2)。答案:(1)丙>甲>乙(2分)(2)①118.62(3分);40%(2分)②135MPa1(3分);>(2分)③>(2分)【23新教材·DY·化学-SJB-选择性必修1-QG】43
本文标签:
起点摸底答案
江西省2023年初中学业水平考试样卷答案