高三2024年普通高等学校招生统一考试 ·最新模拟卷(四)4理科综合ZS4答案

高三2024年普通高等学校招生统一考试 ·最新模拟卷(四)4理科综合ZS4答案,目前趣答答案已经汇总了高三2024年普通高等学校招生统一考试 ·最新模拟卷(四)4理科综合ZS4答案的各科答案和试卷,获取更多{{papers_name}}答案解析,请在关注本站。
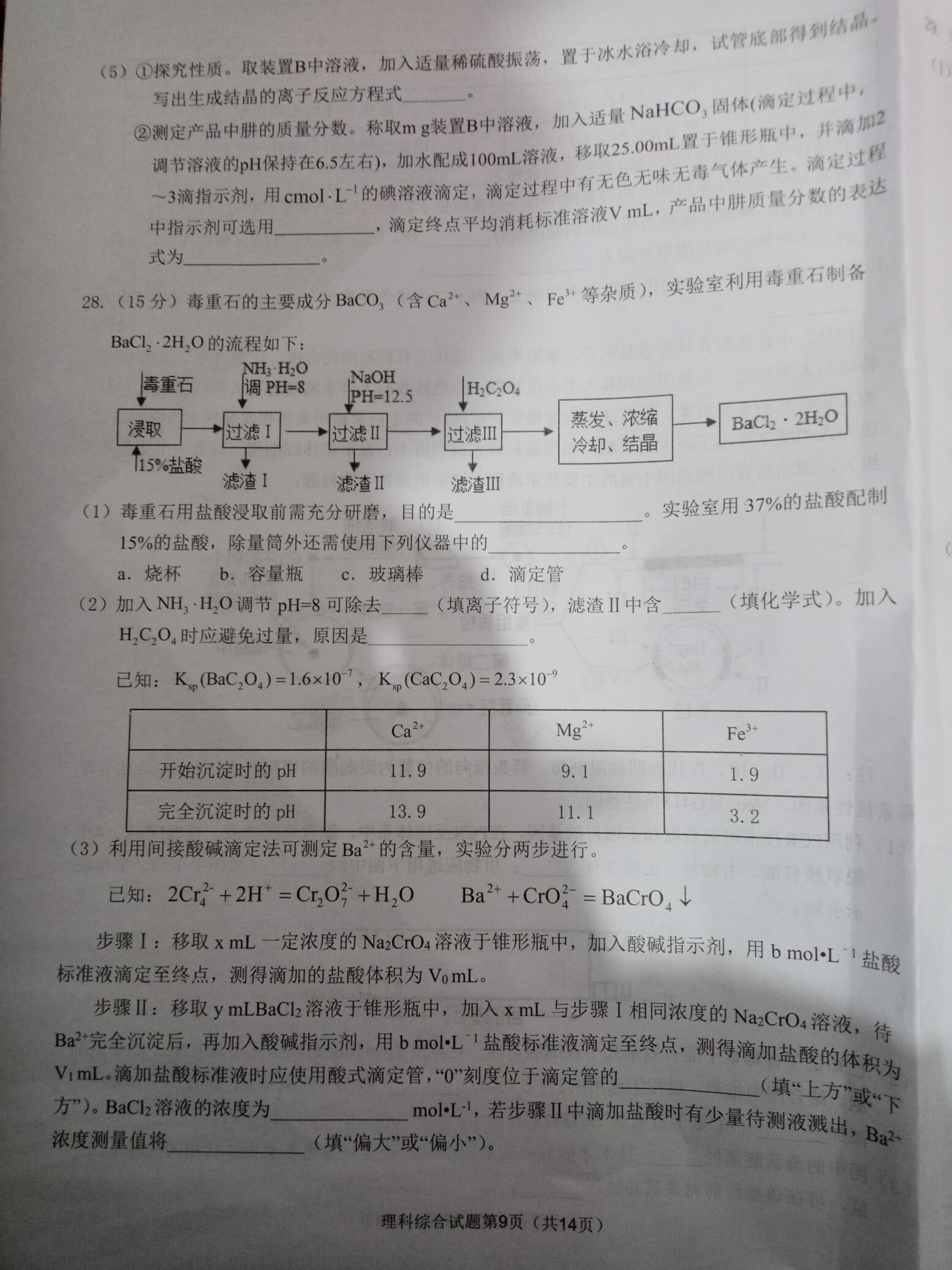 )①探究性质,取装置B中溶液,加入适量稀硫酸振荡。置于冰水浴冷知,试管底郁得到结品②测定产品中肼的质量分数。称取mg装置B中溶液,加入适量NaHCO,固体(滴定过程中写出生成结晶的离子反应方程式调节溶液的pH保持在65左右),加水配成10nL溶液,移取2500mL置于维形瓶中,并清加2一3滴指示剂,用cm01L的膜溶液滴定,滴定过程中有无色无味无毒气体产生。滴定过程中指示剂可选用滴定终点平均消耗标准溶液VmL,产品中肼质量分数的表达式为28(15分)毒重石的主要成分BaC0,(含Ca、Mg、Fe·等杂质),实验室利用毒重石制备BaCL,·2H,O的流程如下:NH;H2O毒重石调PH=8NaOHPH-=12.5H2C204浸取过滤1过滤Ⅱ蒸发、浓缩+过滤BaC2·2HO冷却、结晶15%盐酸滤渣I滤渣Ⅱ滤渣I(1)毒重石用盐酸浸取前需充分研磨,目的是实验室用37%的盐酸配制15%的盐酸,除量筒外还需使用下列仪器中的a.烧杯b.容量瓶c.玻璃棒d.滴定管(2)加入NH,·H,O调节pH=8可除去(填离子符号),滤渣Ⅱ中含(填化学式)。加入HC,O,时应避免过量,原因是已知:K.p(BaC204)=1.6×107,Km(CaC20,)=2.3×109Ca2Mg2Fe3+开始沉淀时的pH11.99.11.9完全沉淀时的pH13.911.13.2(3)利用间接酸碱滴定法可测定Ba+的含量,实验分两步进行。已知:2Cr+2H=CrO2+H,0Ba2++CrO}=BaCr0,↓步骤1:移取xmL一定浓度的Na,CrO,溶液于锥形瓶中,加入酸碱指示剂,用molL1盐酸标准液滴定至终点,测得滴加的盐酸体积为VomL。步骤:移取ymLBaCl溶液于锥形瓶中,加入xmL与步聚】相同浓度的Na,CO,溶液,待B时完全沉淀后,再加入酸碱指示剂,用bm©L盐酸标准液湾定至终点、测得滴加盐酸的体积为V1mL。滴加盐酸标准液时应使用酸式滴定管,“0刻度位于滴定管的方”)。BaCl2溶液的浓度为(填“上方”或“下浓度测量值将moL以,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2(填“偏大”或“偏小”)。理科综合试题第9页(共14页)
)①探究性质,取装置B中溶液,加入适量稀硫酸振荡。置于冰水浴冷知,试管底郁得到结品②测定产品中肼的质量分数。称取mg装置B中溶液,加入适量NaHCO,固体(滴定过程中写出生成结晶的离子反应方程式调节溶液的pH保持在65左右),加水配成10nL溶液,移取2500mL置于维形瓶中,并清加2一3滴指示剂,用cm01L的膜溶液滴定,滴定过程中有无色无味无毒气体产生。滴定过程中指示剂可选用滴定终点平均消耗标准溶液VmL,产品中肼质量分数的表达式为28(15分)毒重石的主要成分BaC0,(含Ca、Mg、Fe·等杂质),实验室利用毒重石制备BaCL,·2H,O的流程如下:NH;H2O毒重石调PH=8NaOHPH-=12.5H2C204浸取过滤1过滤Ⅱ蒸发、浓缩+过滤BaC2·2HO冷却、结晶15%盐酸滤渣I滤渣Ⅱ滤渣I(1)毒重石用盐酸浸取前需充分研磨,目的是实验室用37%的盐酸配制15%的盐酸,除量筒外还需使用下列仪器中的a.烧杯b.容量瓶c.玻璃棒d.滴定管(2)加入NH,·H,O调节pH=8可除去(填离子符号),滤渣Ⅱ中含(填化学式)。加入HC,O,时应避免过量,原因是已知:K.p(BaC204)=1.6×107,Km(CaC20,)=2.3×109Ca2Mg2Fe3+开始沉淀时的pH11.99.11.9完全沉淀时的pH13.911.13.2(3)利用间接酸碱滴定法可测定Ba+的含量,实验分两步进行。已知:2Cr+2H=CrO2+H,0Ba2++CrO}=BaCr0,↓步骤1:移取xmL一定浓度的Na,CrO,溶液于锥形瓶中,加入酸碱指示剂,用molL1盐酸标准液滴定至终点,测得滴加的盐酸体积为VomL。步骤:移取ymLBaCl溶液于锥形瓶中,加入xmL与步聚】相同浓度的Na,CO,溶液,待B时完全沉淀后,再加入酸碱指示剂,用bm©L盐酸标准液湾定至终点、测得滴加盐酸的体积为V1mL。滴加盐酸标准液时应使用酸式滴定管,“0刻度位于滴定管的方”)。BaCl2溶液的浓度为(填“上方”或“下浓度测量值将moL以,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2(填“偏大”或“偏小”)。理科综合试题第9页(共14页)
本文标签: